
DISORDINI FUNZIONALI GASTROINTESTINALI DEL BAMBINO: VI È UN RUOLO DEL MICROBIOTA INTESTINALE?
I disturbi funzionali dell’intestino sono definiti come una combinazione variabile di sintomi cronici o ricorrenti a carico del tratto gastrointestinale in assenza di evidenti alterazioni anatomiche o biochimiche/metaboliche. A differenza di quanto avveniva in passato, la diagnosi di tali disturbi in età pediatrica non necessita più di valutazioni strumentali o di laboratorio, soprattutto in seguito all’introduzione nella pratica clinica, da oltre un decennio, di criteri esclusivamente clinici, i ben noti Criteri di Roma III: la classificazione dei disturbi funzionali dell’intestino, infatti, si basa sui sintomi riferiti dai bambini o dai loro genitori a livello dei cosiddetti organi bersaglio. Tali criteri sono stati pensati per essere utilizzati non solo come strumento diagnostico conveniente e di facile utilizzo, ma anche per pianificare l’approccio terapeutico più adatto al paziente.
Nell’ambito dei disturbi funzionali dell’intestino dei bambini più grandi e degli adolescenti si riconoscono numerosi quadri clinici diversi tra loro (Tabella 1), per ognuno dei quali sono stati realizzati criteri specifici per definirne le caratteristiche cliniche e fisiopatologiche.
TABELLA 1. Classificazione dei disturbi gastrointestinali funzionali |
Uno dei quadri più significativi e rilevanti dal punto di vista clinico è la cosiddetta sindrome del vomito ciclico (SVC), che rappresenta una condizione caratterizzata da crisi di vomito ricorrenti e auto-limitantesi, spesso a carattere stereotipato, intense, nella maggior parte dei casi a carattere biliare, con nausea, fotofobia e talvolta emicrania ed alterazioni della coscienza. Tale condizione rappresenta, nelle forme gravi e recidivanti, una situazione clinica fortemente invalidante per il paziente e la sua famiglia. La prevalenza della SVC rimane comunque piuttosto bassa, compresa tra lo 0.04% e il 2% in età pediatrica, e la condizione tende a manifestarsi più frequentemente nel sesso femminile.
Secondo la classificazione Roma III, per la diagnosi di sindrome del vomito ciclico è necessario che siano soddisfatti entrambi i seguenti criteri:
1. due o più episodi di intensa nausea e vomito incoercibile della durata di ore o giorni;
2. ritorno al normale stato di salute per settimane o mesi (ripristino del peso normale e dell’appettito, ritorno allo stato iniziale di benessere).
La differenziazione tra un pattern ciclico di vomito dal vomito cronico rappresenta un elemento fondamentale nella diagnosi, poiché spesso la SVC è ampiamente sottostimata o mal diagnosticata. In primo luogo, quindi, è necessario ricostruire dettagliatamente i pattern con cui si manifestano gli episodi e successivamente escludere possibili cause organiche, non funzionali, di vomito, che includono sia patologie gastroenterologiche, urologiche (uropatia ostruttiva), endocrine e congenite del metabolismo, sia malattie del sistema nervoso quali, ad esempio, patologie endocraniche (gliomi del tronco), vestibolite, disautonomia familiare.
La terapia nell’attacco acuto mira soprattutto al controllo degli episodi di nausea e vomito e al mantenimento delle perdite di liquidi ed elettroliti.
La profilassi si basa essenzialmente su modificazioni dello stile di vita per 1-2 mesi o 1-2 cicli e la supplementazione di carboidrati.
Altro importante problema clinico è costituito dal dolore addominale funzionale (DAF), che da solo rappresenta il 20-30% delle richieste di visita. A tale proposito è opportuno ricordare la necessità di escludere anzitutto una patologia organica, verificando i sintomi ed i segni di allarme riportati di seguito:
• Dolore persistente all’ipocondrio destro o in fossa iliaca destra
• Disfagia
• Vomito persistente
• Sanguinamento gastrointestinale
• Diarrea notturna
• Familiarità positiva per malattia infiammatoria cronica intestinale, celiachia, patologia peptica
• Dolore che provoca il risveglio del paziente
• Artrite
• Patologia perianale (ragadi, fistole, ascessi)
• Perdita di peso non provocata da dieta ipocalorica
• Rallentamento della crescita
• Ritardo puberale
• Febbre di origine sconosciuta.
Se presenti, questi condurranno necessariamente ad ulteriori indagini volte a diagnosticare la patologia sottostante. In tutti gli altri casi – di gran lunga i più frequenti – occorrerà invece indirizzarsi verso un DAF. A tal proposito si sottolinea l’importanza di diagnosticare a livello ambulatoriale un DAF per evitare di ricorrere ad esami e visite specialistiche inutili.
Il grande polimorfismo dei sintomi, la variabilità nel fenotipo generale, la scarsa classificabilità delle popolazioni, hanno indotto gli Autori dei Criteri di Roma a suddividere le presentazioni cliniche del dolore addominale cronico in quattro aree:
• dispepsia funzionale
• sindrome dell’intestino irritabile
• emicrania addominale
• sindrome dolorosa addominale funzionale dell’infanzia.
Attualmente il DAF è definito come qualsiasi episodio di dolore addominale che sia parzialmente invalidante per la vita del bambino e che non ha criteri sufficienti per essere classificato in un altro quadro clinico di patologia gastrointestinale qui di seguito riassunti:
• dolore addominale episodico o continuo
• criteri che non soddisfano gli altri quadri funzionali
• non evidenza di processi infiammatori, anatomici, metabolici o neoplastici correlabili alla sintomatologia.
Una delle principali cause correlate all’insorgenza di DAF è la sindrome dell’intestino irritabile (SII), la cui prevalenza negli USA è tra il 22 e il 45% dei soggetti fra 4 e 18 anni riferiti a strutture di III livello.
La SII è una delle più frequenti condizioni per le quali si richiede controllo medico, e di conseguenza è molto importante saper riconoscere un bambino con un quadro clinico di questo tipo, in assenza di sintomi di allarme, per avviare precocemente la terapia più adatta. I criteri diagnostici sono menzionati in tabella 2.
TABELLA 2. Criteri diagnostici per la sindrome da dolore addominale dell’infanzia |
L’eziopatogenesi della SII non è ancora completamente nota. Una delle teorie più accreditate riguarda il fenomeno dell’ipersensibilità viscerale, secondo la quale nel soggetto con SII si osserva una iperfunzione delle fibre nocicettive della parete intestinale causata da uno stato di infiammazione cronica: in tal senso stimoli che in un soggetto normale non provocano alcuna sintomatologia, nel paziente con SII provocano dolori e alterazioni della defecazione.
Negli ultimi anni, inoltre, diversi studi e ricerche hanno evidenziato che anche variazioni del microbiota intestinale possono influire sulla funzione del sistema neuromuscolare dell’intestino, con modificazioni della motilità, della percezione viscerale del dolore e della funzione neuromotoria enterica. Ciò è stato dimostrato nel contesto della cosiddetta SII “post-infettiva”, che insorge dopo un episodio di gastroenterite o un’altra infezione. In particolare, nel colon irritabile si può riscontrare un diverso contenuto di idrogeno e metano, correlato a mutamenti della fermentazione batterica e a riduzione di ceppi quali i lattobacilli e bifidobatteri ed aumento di altri, quali i clostridi.
Le raccomandazioni disponibili per la gestione del bambino con dolore addominale cronico, prevalentemente basate sull’opinione di esperti, suggeriscono quindi di indagare la presenza di sintomi e/o segni di allarme in assenza dei quali ulteriori approfondimenti diagnostici non sembrano essere giustificati.
Riuscire ad inquadrare il disturbo del bambino in un modello disfunzionale più preciso può, infatti, aiutare il clinico non solo nella spiegazione del problema ai genitori ed al bambino stesso, ma anche nel trovare l’approccio diagnostico e terapeutico più razionale ed efficace. Il ricorso ad indagini ematochimiche e/o strumentali al fine di escludere patologie organiche è ampiamente dibattuto; in linea generale potrebbe essere raccomandabile la prescrizione di indagini di I livello (emocromo, VES, GOT, GPT, gGT, amilasemia, ricerca sangue occulto nelle feci, anti trans-glutaminasi tissutali, esame urine e coltura, coprocoltura ed esame parassitologico feci, ecografia addominale e pelvica), procrastinando l’esecuzione di ulteriori esami di approfondimento solo in presenza di segnali di allarme (anticorpi ASCA e ANCA, calprotectina fecale, urea breath test, pH-metria delle 24 ore, EGDS, colonscopia, test di intolleranza al lattosio) e/o in base all’evoluzione clinica del quadro sintomatologico.
Per quanto riguarda l’approccio terapeutico, nella pratica corrente in età pediatrica l’atteggiamento più diffuso prevede un trattamento empatico con la rassicurazione del paziente e della famiglia e che si associa ad una risoluzione dei sintomi nel 30-40% dei casi, prevalentemente nei casi di dolore addominale cronico funzionale. Nei casi più complessi, la strategia terapeutica del dolore addominale funzionale prevede tre differenti approcci: farmacologico, dietetico e psicologicocomportamentale. In merito alla terapia farmacologica, solo tre studi hanno valutato l’uso di farmaci in bambini con DAF e riguardano l’uso della famotidina in bambini con dispepsia funzionale, del pizotifene nell’emicrania addominale e dell’olio di menta piperita nella SII. Nonostante nella pratica clinica si utilizzino molti farmaci per la gestione dei sintomi associati al dolore addominale ricorrente, quali anti-colinergici, anti-emetici, anti-spastici, anti-depressivi, simeticone, analgesici, cromoglicati ed estratti di erbe, nessuno studio ha dimostrato l’efficacia nei disturbi funzionali del tratto gastroenterico del bambino. L’olio di menta piperita si è dimostrato più efficace del placebo nel ridurre la frequenza e l’intensità della sintomatologia dolorosa nei bambini con SII, probabilmente grazie all’azione miorilassante del mentolo che agisce come inibitore dei canali del calcio e riduce la motilità intestinale ed ai possibili effetti anestetico, topico ed antibatterico. La supplementazione con fibre, pur non risultando efficace nella terapia del DAF, rappresenta un corretto supplemento alimentare nella popolazione pediatrica.
I probiotici, infine, rappresentano una promettente terapia in grado di modificare i sintomi e il decorso della malattia: esperienze cliniche dimostrano infatti che il consumo di probiotici è più efficace del placebo nel determinare un migliore controllo del dolore (frequenza ed intensità) alla fine del trattamento e soprattutto durante il follow-up.
Uso dei probiotici nell’ambulatorio del pediatra
Le evidenze a favore dell’uso dei probiotici derivano da un grande numero di studi scientifici pubblicati: soltanto nell’ultimo anno, infatti, sono presenti in oltre 800 lavori condotti su molteplici e differenti patologie. Il grande interesse da parte dei ricercatori è indubbiamente da correlare all’importanza che riveste il microbiota intestinale sia per la salute umana che per le malattie; è un concetto in realtà noto già da oltre un secolo. Ciò non è affatto sorprendente se si considera che l’area totale della mucosa gastrointestinale umana in un adulto occupa una superficie che può arrivare fino a 300 m², rendendola in tal modo la più estesa zona del corpo in grado di interagire con l’ambiente, e soprattutto tenendo conto dell’enorme numero di microrganismi presenti nell’intestino (circa 1014), corrispondenti ad oltre 10 volte il numero totale di cellule dell’organismo.
Il termine “probiotico” fu coniato nel 1965 da Lilly e Stillwell, con accezione opposta a quella di antibiotico, per indicare l’effetto stimolante sulla crescita batterica da parte di sostanze rilasciate da microrganismi. Attualmente si parla di probiotici riferendosi a qualsiasi prodotto che contenga lattobacilli mentre il termine probiotico si dovrebbe riferire solo a prodotti che contengono i ceppi che soddisfano determinati requisiti contenuti nelle Linee Guida Ministeriali che fanno riferimento alle Linee Guida WHO-FAO (Tabella 3).
TABELLA 3. Requisiti per la definizione dei probiotici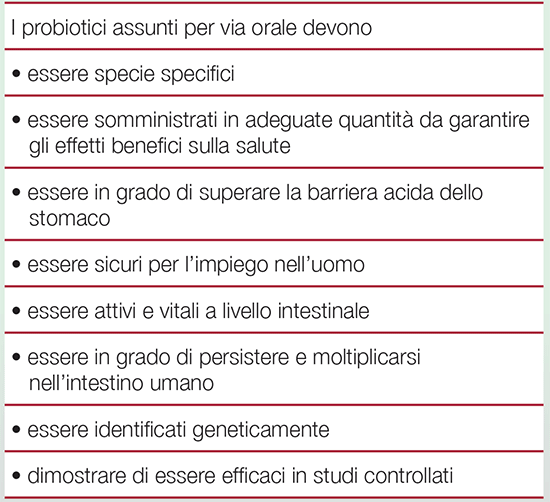 |
Per una corretta scelta ed un adeguato uso dei probiotici è essenziale la caratterizzazione genetica e la definizione di ogni ceppo: ogni specie di batteri, infatti, comprende ceppi diversi in grado di determinare benefici differenti: ogni specifico ceppo possiede specifiche attività e differenti effetti benefici. Solo la caratterizzazione a livello genetico consente di attribuire correttamente le proprietà di un determinato probiotico.
Nella comunità scientifica esiste dunque una nomenclatura riconosciuta per i microrganismi, in cui ogni ceppo viene classificato in base al genere e alla specie, ed è associato ad un codice alfanumerico. Tale metodologia viene effettuata in quanto gli effetti descritti possono essere attribuiti solo al ceppo o ai ceppi testati, e non alle specie o all’intero gruppo di batteri (ad esempio lattobacilli) o di altri probiotici.
La sola corretta caratterizzazione non rappresenta tuttavia una garanzia sufficiente per l’utilizzo di un probiotico, in quanto è necessario tenere in considerazione altri fattori. Anzitutto gli effetti sulla salute di un ceppo devono essere documentati, e i risultati di studi su ceppi specifici non possono essere utilizzati su ceppi non testati.
L’efficacia di ceppi specifici in una determinata dose, inoltre, non è sufficiente per provare gli effetti sanitari di un dosaggio minore.
Diversi studi confermano che per alcune patologie sia i Lattobacilli che i Bifidobatteri possono avere effetti clinici in diverse condizioni cliniche in età pediatrica. Per alcune di queste condizioni l’efficacia è ben documentata da tempo, ad esempio nella riduzione della durata della diarrea infettiva in neonati e bambini, nella prevenzione dell’enterocolite necrotizzante e nella riduzione della diarrea associata al trattamento antibiotico.
Sulla base di queste premesse è stata condotta una ricerca sulla popolazione pediatrica che afferisce agli ambulatori dei pediatri del territorio per problemi gastrointestinali per verificare l’utilizzo dei probiotici.
La ricerca ha coinvolto 38 pediatri di base in 9 regioni italiane, allo scopo di valutare mediante una semplice “scheda paziente” gli effetti di alcuni probiotici sulla sintomatologia di diversi disturbi gastrointestinali dopo 2 settimane di trattamento.
Dopo aver verificato il rispetto dei requisiti ministeriali, i ceppi probiotici utilizzati sono stati il Lactobacillus salivarius I-1794 e il Lactobacillus paracasei I-1688 in rapporto12:1 (PSmix®).
La ricerca ha incluso complessivamente 1365 bambini (Tabella 4).
TABELLA 4. Caratteristiche demografiche dei bambini inclusi nello studio |
La valutazione delle cause che hanno motivato la somministrazione (Tabella 5) ha confermato come proprio il dolore addominale rappresenti il sintomo in assoluto più frequentemente riportato (65.2%), sottolineando ancora una volta la significativa prevalenza di questo disturbo e il suo impatto sulla qualità di vita del bambino e della famiglia, ancor più di altri quali diarrea, gonfiore e flatulenza. Il dolore addominale, infatti, nel 50% dei bambini di tipo funzionale, risultava presente da 3 a 5 volte a settimana in quasi la metà dei casi, e con elevata frequenza (≈40%) anche durante le ore notturne.
TABELLA 5. Cause che hanno motivato la somministrazione della miscela di probiotici |
Inoltre, al momento del reclutamento, circa la metà dei bambini presentava <5 evacuazioni settimanali e solo il 26.4% riportava feci di consistenza normale.
La somministrazione della miscela di probiotici PSmix® 1 bustina/die (carica batterica nlt 109 UFC) bis in die per 15 giorni ha determinato una significativa riduzione della frequenza del dolore addominale (Figura 1), che si è ridotto dal 73.1% (n=910) al 13.6% (n=182); analogamente, è stata osservata una significativa riduzione dei dolori notturni.
È stato inoltre rilevato un aumento del numero di evacuazioni settimanali (Figura 2), con conseguente rilevante regolarizzazione dell’alvo. La somministrazione di probiotici ha favorito altresì un aumento della consistenza della massa fecale: la percentuale di feci normali è salita ad oltre l’80% (81.5%), con parallela riduzione delle feci liquide o molli dal 48.7% a <10% (9.7%) (Figura 3).
I risultati di questa indagine hanno confermato quindi che un adeguato periodo di trattamento con una miscela selezionata di probiotici Lactobacillus salivarius I-1794 e Lactobacillus paracasei I-1688 in rapporto 12:1 (PSmix®) favorisce:
• il miglioramento della consistenza delle feci
• la riduzione del dolore addominale ricorrente
• la normalizzazione del numero di evacuazioni settimanali.
FIGURA 1. Percentuale di bambini con Dolore Addominale Ricorrente (DAR). |
Tali sintomi rientrano nei criteri diagnostici del DAF (vedi tabella 2), i dati raccolti costituiscono pertanto una ulteriore conferma che determinati ceppi probiotici risultano un valido supporto nella gestione del paziente con disturbi gastrointestinali.
FIGURA 2. Percentuale di bambini con numero di evacuazioni settimanali comprese tra 3 e 5.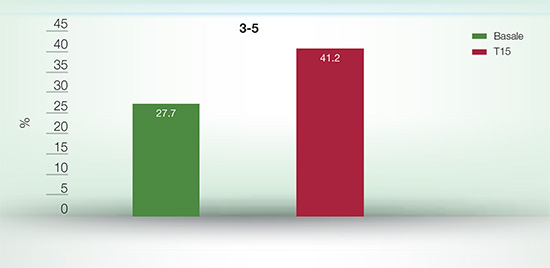 |
Va inoltre sottolineato che, data l’importanza che riveste il microbiota intestinale nella fisiologia dell’organismo, le potenzialità dei probiotici sono ancora un’area da esplorare: i campi di applicazione dei probiotici in futuro potrebbero non limitarsi alle sole patologie intestinali. Infatti, sono allo studio ulteriori campi di applicazione dei probiotici (allergie respiratorie, prevenzione dermatite atopica) i cui risultati sono molto promettenti. Le attuali evidenze ci suggeriscono come la prima infanzia sia un periodo critico per la modulazione della microflora intestinale, e pertanto è ragionevole suggerire che eventuali prove di efficacia dei probiotici dovrebbero essere effettuate proprio durante il periodo dell’infanzia, in cui è maggiormente probabile osservare significativi benefici sia clinici che in termini di qualità della vita.
FIGURA 3. Consistenza delle feci al basale e dopo 15 giorni di trattamento.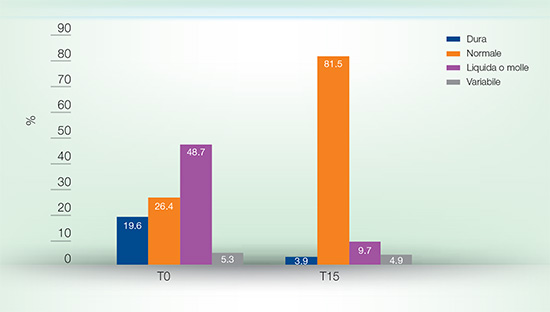 |
|